
퇴적물 기반 미세플라스틱이 해양 단각류(Monocorophium uenoi)에 미치는 세대 간 생식 독성
초록
본 연구는 미세플라스틱의 퇴적물 침적이 해양 저서성 무척추동물의 생식에 미치는 영향을 평가하기 위해 수행되었다. 실험에는 해양 단각류 Monocorophium uenoi를 모델 생물로 사용하였으며, 미세플라스틱(PET)을 서식 기질로 대체한 장기 노출 실험을 통해 급성독성 및 생식력(fecundity)에 대한 영향을 확인하였다. 급성 노출(96시간)에서는 유의한 생존율 감소가 관찰되지 않았으나, 1세대의 만성 노출(28일) 시 자손 생산은 대조군 대비 약 55% 수준으로 감소하였다. 2세대의 만성 노출 시 암컷 단독 노출군과 암수 모두 노출군에서 정량적으로 자손 생산이 완전히 억제되었다. 조직 및 장기 내 미세플라스틱은 라만분광법(Raman spectroscopy)을 통해 확인하였으며, 이러한 생식 독성이 미세플라스틱의 물리적 존재와 연관됨을 뒷받침하였다. 본 연구는 퇴적물 내 미세플라스틱이 단순 입자성 물질의 단기적 생존 영향을 넘어, 여러 세대에 걸쳐 단각류의 생식 능력을 완전히 상실시킬 수도 있는 잠재적 위협임을 실증하였다.
Abstract
This study was conducted to evaluate the effects of sediment-associated microplastics on the reproduction of marine benthic invertebrates. The marine amphipod Monocorophium uenoi was used as a model organism, and the impacts on acute toxicity and fecundity were investigated through a long-term exposure experiment in which polyethylene terephthalate (PET) microplastics replaced the natural habitat substrate. While no significant decrease in survival was observed in the 96-hour acute exposure, a 28-day chronic exposure to the first generation (F1) resulted in a reduction of offspring production to approximately 55% of the control group. In the subsequent chronic exposure of the second generation (F2), offspring production was completely inhibited in groups where either only females or both sexes were exposed. The presence of microplastics within tissues and organs was confirmed via Raman spectroscopy, supporting the link between the physical presence of microplastics and the observed reproductive toxicity. This study demonstrates that sediment-associated microplastics are more than just inert particles affecting short-term survival; they represent a potential threat capable of causing a complete loss of the reproductive capacity in amphipods across multiple generations.
Keywords:
Microplastic, Benthic amphipod, Reproductive toxicity, Transgenerational toxicity키워드:
미세플라스틱, 단각류, 생식 독성, 세대 간 독성1. 서 론
미세플라스틱(Microplastic, MP)은 5 mm 미만의 합성 고분자 입자로, 산업 활동과 플라스틱 폐기물의 물리·화학적 파편화 과정을 통해 해양, 담수, 육상 등 전 지구적 생태계에 광범위하게 축적되고 있다(GESAMP[2015]). 특히 해양 환경으로 유입된 미세플라스틱은 낮은 비중으로 인해 수중에 부유하기도 하지만, 상당수는 생물 분비물이나 유기물과 응집하여 해저 퇴적물에 축적되는 경향을 보인다. 이로 인해 퇴적물은 수중 환경보다 훨씬 높은 농도의 미세플라스틱을 함유하는 '오염의 저장고(sink)'가 되며, 이곳을 주된 서식지로 삼는 저서생물군(benthic organisms)에게는 피할 수 없는 장기적 위협 요인으로 작용한다(Wang et al.[2021]).
생물에 의한 MP 섭취 및 체내 축적 현상은 초기 연구부터 명확히 규명되었다. 담치(Mytilus edulis)를 이용한 선구적인 연구들은 섭취된 MP가 단순히 소화관에 머무는 것이 아니라, 소화관 벽을 통과하여 순환계와 다른 조직으로까지 이동(translocation)하며(Browne et al.[2008]), 조직 수준에서 염증반응과 같은 심각한 세포 독성을 유발할 수 있음을 증명하였다(von Moos et al.[2012]). 이러한 발견 이후, MP 섭취와 그로 인한 생물학적 영향은 저서성 무척추동물부터(Windsor et al.[2019]) 어류, 해양 파충류, 조류, 포유류에이르기까지(e.g., Jovanović et al.[2017]; Duncan et al.[2019]; Nelms et al.[2019]) 해양 생태계 전반의 다양한 분류군에서 광범위하게 보고되고 있으며(Barboza et al.[2020]), 수서 생태계 여러 생물에도 해당한다(Hu et al.[2018]; McNeish et al.[2018]). 이는 MP가 먹이망을 통해 전달될 수 있는 잠재적 위험 인자임을(da Costa Araujo et al.[2020]; [2021]), 그리고 해양 상위 포식자에서 미세플라스틱 섭취 빈도가 높고 예측 가능한 요인 존재를 시사한다(Kühn et al.[2015]).
해양퇴적물에 분포하는 MP가 저서생물에 미치는 영향은 크게 물리적, 화학적 측면으로 구분할 수 있다. 물리적으로, 섭취된 MP는 생물의 소화기관을 막거나 손상하고, 거짓 포만감을 유발하여 정상적인 영양 섭취를 방해함으로써 성장을 저해한다(Green[2016]). 특히 갯지렁이(Arenicola marina)와 같은 퇴적물 섭식자는 오염된 환경에서 굴착 및 섭식 행동이 현저히 감소하여 에너지 고갈을 겪는 것으로 보고되었다(Green et al.[2019]). 화학적으로는 플라스틱 제조 시 첨가된 가소제, 비스페놀 A(BPA) 등의 유해 첨가제가 체내로 용출되어 내분비계를 교란하고 생식 기능을 직접적으로 손상시킬 수 있다(Coady et al.[2017]; Hermabessiere et al.[2017]). 실제로 폴리스티렌 MP에 노출된 굴(Crassostrea gigas)은 생식세포 형성과 배아 발달에 심각한 저해를 받는 것으로 확인되었다(Sussarellu et al.[2016]).
이처럼 미세플라스틱의 유해성에 대한 연구가 활발히 진행되고 있음에도 불구하고, 상대적으로 작은 입자를 대상으로 한 단기간의 생존율 변화에 초점을 맞춘 급성독성 평가나 단일 세대 내에서의 생리적 변화 관찰에 집중되는 경향이었다. 그러나 생태계에 미치는 실질적인 위협은 개체수준의 생존 여부보다는, 세대를 거치며 누적될 수 있는 아급성 영향(sub-lethal effect), 특히 개체군의 존속과 직결되는 생식력(fecundity) 저하에 있을 수 있다. 해산 요각류를 모델로 하여 섭식 감소, 생식률 저하, 생장 지연을 미세플라스틱 농도에 따라 정량 분석한 결과 번식력 저해와 유생발달 지연 연구(Jeong et al.[2020]) 이후 최근 연구에서 나노플라스틱이 요각류의 여러 세대에 걸쳐 후성유전학적 교란을 통해 생식 기능을 완전히 상실시킨다는 결과가 보고되면서(Zhao et al.[2023]), 미세플라스틱의 ‘세대 간 독성(transgenerational toxicity)’에 대한 규명이 시급한 문제로 떠올랐다. 하지만 저서 환경에서 미세플라스틱이 여러 세대에 걸쳐 생식에 미치는 영향을 직접적으로 규명한 연구는 여전히 매우 부족하다.
따라서 본 연구는 해양 저서 생태계의 주요 구성원인 단각류 Monocorophium uenoi를 모델 생물로 사용하여 퇴적물 기반 미세플라스틱(PET, polyethylene terephthalate)에 대한 장기적, 만성 노출이 생식 능력에 미치는 영향을 여러 세대에 걸쳐 평가하고자 하였다. 이를 통해 미세플라스틱이 단일 개체의 생존을 넘어 세대 간 생식 연속성을 저해함으로써 개체군 수준에 미칠 수 있는 잠재적 위험성을 실증적으로 규명하고자 하였다.
2. 재료 및 방법
시험은 다양한 농도로 조제된 MPs 현탁액에 세가시육질꼬리옆새우, M. uenoi를 노출하여 생존(사망)을 관찰하였다. 시험생물은 해양환경공정시험기준(National Institute of Fisheries Science[2023])에 제시된 표준시험생물로서 실험실 내 계대 배양하는 개체를 사용하였다.
시험에 사용된 미세플라스틱은 한국생산기술연구원(KITECH)에서 독성시험용 표준물질로 제공받았다. 해당 물질은 폴리에틸렌 테레프탈레이트(Polyethylene terephthalate, PET)를 동결분쇄(Cryomilling) 및 입자 분급(Sieving) 기술을 통해 파편(fragment) 형태로 제조한 것이다(Chae et al.[2025]). 모든 입자는 전자현미경 분석을 통해 형태와 크기가 검증되었으며, 본 연구에서는 15–20 μm와 45–75 μm의 두 가지 크기 구간을 사용하였다.
2.1 시료의 준비
250-ml 유리 비커 4개에 MPs 현탁액을 각각 200 ml 씩 주입하여 준비하였고 1-μm 유리섬유 필터로 여과한 해수(여과해수)를 채워 음성대조구로 준비하였다. MPs 현탁액은 파편형 PET 15-20 μm 0.1002 g을 20 ml 용량의 유리 바이알에 10 ml의 여과해수와 혼합하여 최고농도로 조제 하였고 절반씩 희석하여 63.0 mg/L 농도 까지 5 개 농도로 준비하였다. 파편형 PET 45-75 μm 0.1022 g을 20 ml 용량의 유리 바이알에 10 ml의 여과해수와 혼합하여 최고농도로 조제 하였고 절반씩 희석하여 63.9 mg/L 농도 까지 5 개 농도로 준비하였다.
만성실험 시료는 1-L 유리 비커에 파편형 15-20 μm와 45-75 μm를 혼합한 MP 시료를 바닥에 골고루 퍼지도록 준비 하였다. 대조구는 1-L 유리 비커에 배양에 사용하는 깨끗한 퇴적물을 넣어 대조구로 준비하였다.
2.2 급성독성 실험
MP의 급성 노출시험은 해양환경공정시험기준, 해양폐기물공정시험기준 ‘제22항 저서성 단각류(Monocorophium)를 이용한 해양배출 폐기물 독성평가 방법’을 준용하였다. 노출 생물은 크기로 구분하였다. 500-μm 표준체를 통과하고 300-μm 표준체에 걸리는 개체를 수거하여 건강한 개체를 선별하여 MP 농도별로 준비된 비커에 10 마리씩 투입하였다. 투입 시점에서 96 시간 동안 20°C로 설정된 항온 배양기에서 노출하였다. 조명, 폭기 그리고 먹이는 없는 조건으로 노출하였다(Table 1). 96 시간 경과 후 대조구의 생존 개체수를 확인하여 시험 적합성을 검토한 후 시험구의 생존 개체수를 기록하여 생존율(사망률)을 구하였다.
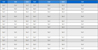
Summary of test conditions for acute toxicity of microplastics on the benthic amphipod, Monocorophium uenoi
2.3 만성독성 실험
만성 노출 실험은 미국 환경보호청(USEPA)의 'Methods for Assessing the Chronic Toxicity of Marine and Esturine Sediment-associated Contaminants with the Amphipod Leptocheirus plumulosus'를 본 연구의 시험종인 Monocorophium uenoi에 맞게 변형하여 적용하였다(USEPA[2001]).
만성실험은 3 단계로, 처음 노출되는 유생을 1 세대(F1)로 하여 생존과 2 세대(F2) 생산력과 F2의 연속 노출로 인한 3 세대(F3) 생산력을 평가하고자 하였다(Fig. 1). 노출 재료는 PET, 파편형, 크기 15-20 μm, 45-75 μm의 MP 입자를 구분하지 않고 모두 섞어 퇴적물처럼 사용하였다. 시험의 대조구는 생물의 배양에 사용되는 오염되지 않은 퇴적물을 사용하였다. 시험생물은 급성독성 실험을 종료한 개체들을 수거하여 급성 실험에서 노출된 농도와 상관없이 모두 섞어 혼합 MP가 기질로 있는 비커에 20 마리씩 투입하였다. 4개의 반복구로 28 일 간 노출하였다. 노출 종료 후 생존 개체를 모두 수거하여 MP 노출 F1 자손을 계수하였다. 대조구도 처리구와 같은 과정으로 실험하였다.
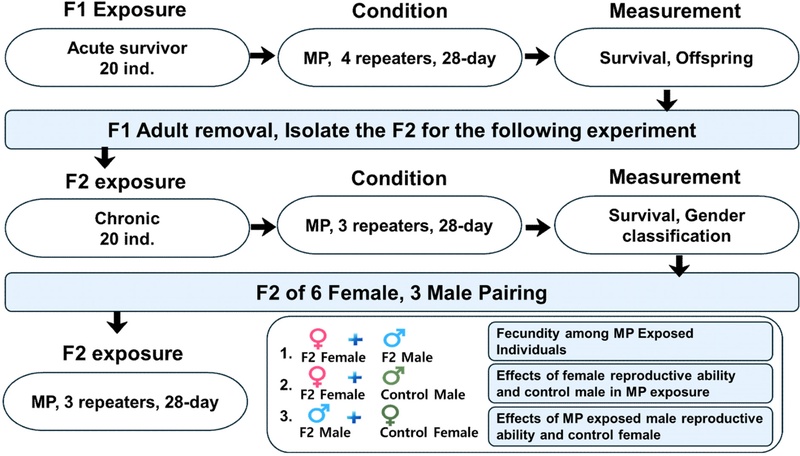
Schematic diagram of the chronic and transgenerational toxicity test design. The first parental generation (F1) was chronically exposed to microplastic (MP) sediment for 28 days. The resulting offspring (F2 generation) were then isolated and subjected to an identical chronic exposure. To investigate gender-specific reproductive impairment, the fecundity of the F2 generation was evaluated through a cross-mating design, which included pairings within the MP-exposed group, as well as reciprocal crosses between MP-exposed and control individuals.
F2를 노출하기 위해 F1 성체를 모두 제거하고 F2만을 혼합 MP가 기질로 있는 비커 3개에 나누어 28 일 간 노출하였다. 노출을 종료하고 노출 개체는 성별로 구분하였다. 암컷 6 마리와 수컷 3마리씩 3 반복으로 28 일 간 다시 노출하여 자손의 생산을 확인하였다. 대조구는 3 반복으로, 반복구 당 대조구에서 수거한 암컷 6마리와 수컷 3 마리씩 투입하였다. 처리구는 MP에 노출된 F2 암컷과 수컷 조합, MP에 노출된 F2 암컷과 대조구의 수컷 조합 그리고 MP에 노출된 F2 수컷과 대조구의 암컷 조합으로 구성하였다.
실험 개체의 성별 구분은 해부 현미경 하에서 두 번째 악지(second gnathopod)의 형태적 차이를 기반으로 수행하였다. 암컷에 비해 크기가 월등히 크고 강건한 집게 형태의 두 번째 악지를 가진 개체를 수컷으로 동정하였고, 자손의 생산은 암컷 한 마리 당 생산한 자손수(Fecundity)로 계산하였다.
2.4 조직 분석
노출 종료 후 라만분광법으로 단각류의 조직 내 MP를 검출하였다. 라만 분석은 절편된 생물 조직 내에서 직접 입자의 정성 동정이 가능하고, 동결 절편은 세척 과정을 통해 Optimal Cutting Temperature compound(OCT; Sakura Finetek, USA) 매질 제거 후에도 라만 신호의 간섭 없이 물질의 피크를 안정적으로 검출할 수 있어 MP의 생체 내 거동을 규명하는 데 중요한 분석 기반이 될 수 있다.
MP에 노출된 단각류 조직 내의 미세플라스틱을 확인하기 위해 냉동 절편을 제작하여 분석하였다. 라만 분광 분석을 위한 조직 시료의 절편 제작은 선행연구(Aeamendia et al.[2024]; Calmao et al.[2023])를 참고하여 다음과 같이 수행하였다. 먼저, 단각류 시료를 Cryomold(크라이오몰드)에 위치시킨 후, OCT를 몰드 절반 높이까지 주입하였다. 시료를 원하는 자세로 배치한 후, 시료가 완전히 잠기도록 OCT를 추가로 부어 덮었다. 조직이 담긴 Cryomold는 –80℃ 에서 급속 동결 시켰으며, 시편은 절편 전까지 동일 온도에서 보관하였다. 조직 절편은 Cryomicrotome(냉동마이크로톰)을 사용하여 –30℃ 이하의 온도에서 진행하였다. 절편된 조직은 일반 슬라이드 글라스에 부착 후 상온에서 OCT를 자연적으로 용해 시켰고, PBS 완충용액(phosphate-buffered saline, pH 7.4)으로 슬라이드를 세척 하여 잔여 OCT를 최대한 제거하였다. 이후 조직 위에 조직 고정용 mounting medium을 떨어뜨리고 cover glass를 덮은 후 4℃에서 보관하며 라만 분석하였다.
3. 결 과
3.1 급성독성
M. uenoi를 대상으로 다양한 농도의 MPs (15–20 μm 및 45-75 μm)을 96시간 동안 노출하여 급성독성 반응을 평가하였다. 일원배치분산분석(One-way ANOVA) 후 Tukey 사후검정(유의수준 p < 0.05)을 실시한 결과, 두 입자 크기에서 모든 처리군과 대조군 간에 유의한 생존율 차이는 나타나지 않았다(Fig. 2). 두 입자 크기 그룹 모두에서 생존율은 90% 이상으로 유지되었으며, 농도 증가에 따른 뚜렷한 용량-반응(dose–response) 경향도 확인되지 않았다.
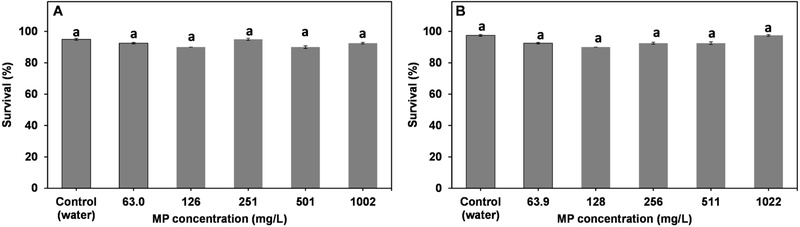
Survival rate (%) of Monocorophium uenoi following a 96-hour acute exposure to PET (polyethylene terephthalate) microplastics at various concentrations. Results are shown for two particle size ranges: (A) 15–20 µm and (B) 45–75 µm. Each bar represents the mean survival rate (%) ± standard deviation (n=4). A one-way ANOVA followed by Tukey's post-hoc test confirmed that there were no statistically significant differences between the control and any microplastic-exposed group (p > 0.05). Bars sharing the same letter (a) are not significantly different.
3.2 만성독성
28 일간의 만성 노출 실험에서는 급성독성과는 명확히 구분되는 결과가 나타났다. 유생 때부터 미세플라스틱에 노출된 F1은 28일 간의 노출 후 생존율은 대조구와 차이가 없었고 기질인 MP를 이용하여 집을 짓고 생활하였으며 자손 또한 생산하였다(Fig. 3).

Photographic of Monocorophium uenoi constructing and residing in a shelter composed entirely of fragment-type microplastics (MPs). (1) a cylindrical MP-based structure, (2) a developed shelter mimicking a natural tube, and (3) an individual inhabiting the MP structure. These observations suggest active behavioral use of MPs as a habitat material.
생산 개체수(Offspring)로 비교하였을 때, F1은 플라스틱에 노출되지 않았던 대조구의 54.9% 수준의 낮은 생산량을 나타내었다(Fig. 4).
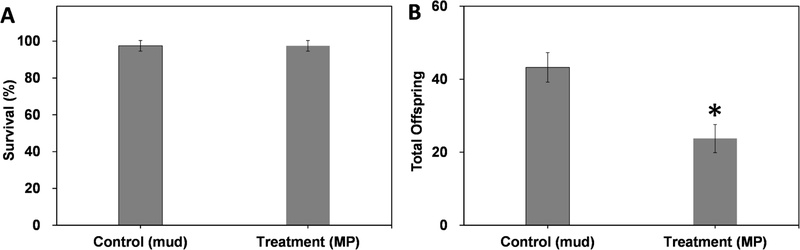
Effects of a 28-day chronic exposure to sediment-associated microplastics on the first generation (F1) of Monocorophium uenoi. (A): the survival rate (%); (B): total number of offspring produced. Data are presented as the mean ± standard deviation (n=4). While the survival rate showed no significant difference between the control (mud) and treatment (MP) groups (t-test, p > 0.05), the total number of offspring was significantly reduced in the treatment group (t-test, p < 0.05). *: significant difference compared to the control group.
그러나 F2는 부모 세대의 노출 및 배아기 이전부터의 간접 영향까지 포함하여 전 생애에 걸쳐 MP에 노출되었으며, 그 결과 생식력(Fecundity) 저하가 뚜렷하게 확인되었다(Fig. 5).
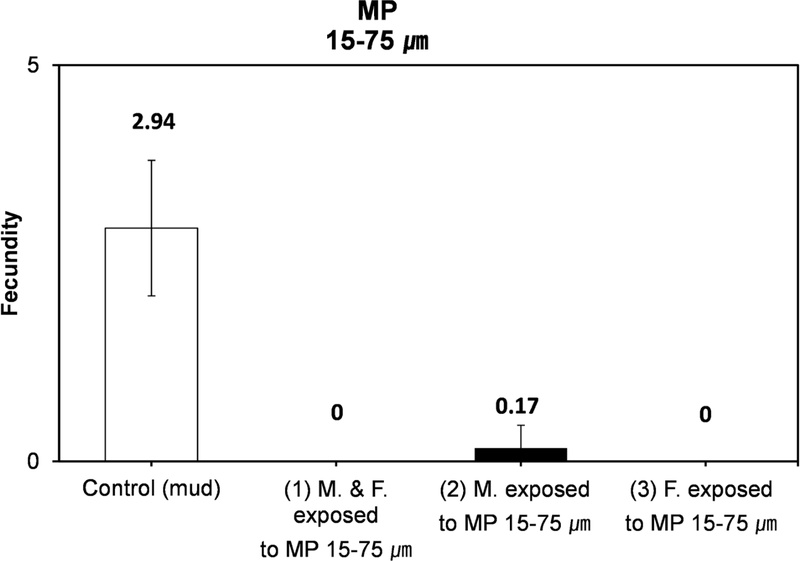
Fecundity of Monocorophium uenoi following chronic exposure to fragment-type microplastics (MPs) (15–75 μm). Test groups included: (1) both male and female exposed to MPs, (2) only males exposed, and (3) only females exposed, with the control group reared in uncontaminated sediments. Compared to the control, fecundity was significantly reduced in all exposed groups.
F2 개체군 중 일부에서 제한적인 생식 기능을 확인하였으나, F3의 출현은 거의 관찰되지 않았으며, 특히 암컷이 노출된 군에서는 자손 생산이 전무하였다. 이는 MP가 생물의 생존에는 직접적인 급성독성을 나타내지 않더라도, 생식 기능 저해를 포함한 만성적인 생리 교란을 유발할 수 있음을 의미한다(Table 3).

Reproductive output and survival rate of Monocorophium uenoi following chronic exposure to fragment-type microplastics (MPs) (15–75 μm). The upper section shows fecundity and survival of the first generation (F1) after 28 days of exposure. The lower section presents offspring production and survival of second-generation (F2) individuals under different mating combinations: both sexes exposed, only males exposed, and only females exposed to MPs. Although all groups exhibited high survival rates (>96%). No offspring were produced when both sexes or only the female were exposed to MPs, whereas the male-exposed-only group showed very limited reproductive success. Data are presented as mean ± standard deviation
3.3 조직 분석
10일간의 급성 노출 후 M. uenoi의 동결 조직 절편 내부에서 축적된 입자를 관찰하였다. 광학현미경으로 단각류 조직의 절편을 관찰한 결과, Section A는 등쪽(몸통 중앙) 부위의 절편 사진이고 상단 패널에서 체내 조직에 박혀있는 어두운 색의 플라스틱 유사 입자들의 응집체가 명확하게 관찰되었다. 하단 패널의 확대 사진은 이 입자들이 조직 내에 존재함을 고배율로 다시 확인하였다. Section B는 머리 부위의 절편 사진으로, 100 배율 사진에서 조직에 축적된 플라스틱과 유사한 입자들을 명확하게 확인할 수 있었다(Fig. 6). 조직 내에 존재하는 입자가 배면 및 두부에서 확인되었으며, 해당 입자들은 크기는 실험에 사용된 10-20 μm 크기의 파편형 MPs와 유사하였다. 단각류 체내입자를 정의하기 위한 라만 분광 분석 결과, 관찰한 절편들의 조직 내 입자에서 PET의 대표적인 Raman 피크가 명확히 검출되었으며, 이는 실험에 사용된 MP 분광 스펙트럼과 일치하였다. 그리고 15-20 μm와 45-75 μm 두 크기 그룹 모두에서 PET의 전형적인 스펙트럼이 확인되었다(Fig. 7). 특히, 에스테르 그룹의 C=O 신축 진동에 해당하는 1730 cm-1 피크와 벤젠고리의 방향족 C-C 신축 진동에 해당하는 1615 cm-1 피크가 매우 강하게 나타나, 해당 물질이 PET임을 명확하게 뒷받침하였다. 이외에도 1290 cm-1, 1120 cm-1, 1095 cm-1 등에서 관찰되는 C-O 결합 관련 피크들이 표준 PET 스펙트럼과 정확히 일치함을 확인하였다. 이러한 결과는 실험군 개체의 생체 내 조직, 특히 소화기관 및 조직 심부에 이들 플라스틱 입자가 실제로 존재함을 명확히 나타내었다.
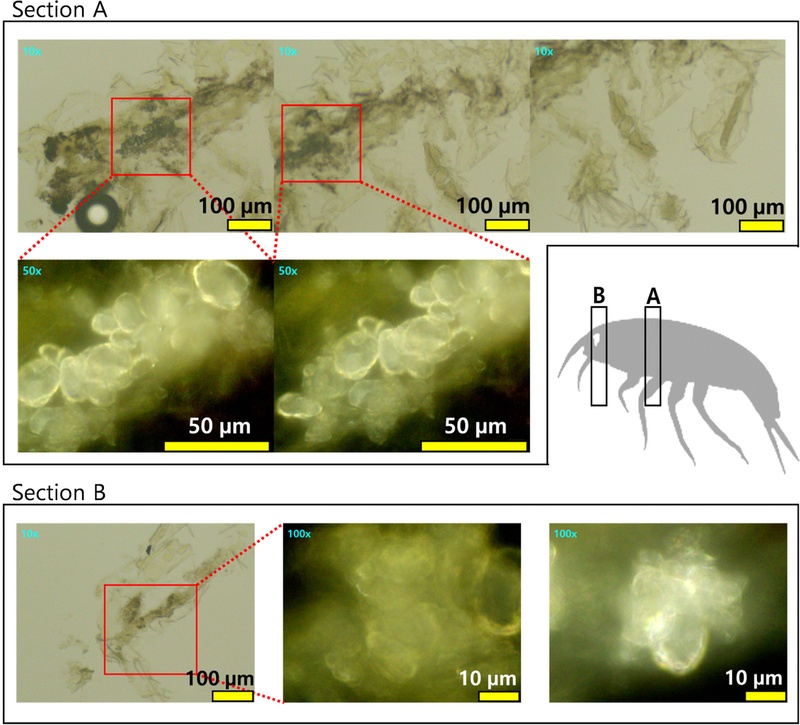
Microscopic evidence of internalized particles within the frozen tissue sections of Monocorophium uenoi after acute exposure. A schematic diagram illustrates the body parts the sections imaged. Section A shows the dorsal (mid-body) region, where aggregates of dark, xenobiotic particles are clearly visible embedded within internal tissues at 10x magnification (top panel). Section B focuses on the head region, showing similar particle accumulation deep within the tissue, which is clearly visible at 100x magnification. Scale bars are indicated in each image.
4. 고 찰
본 연구는 퇴적물에 존재하는 PET 미세플라스틱이 해양 저서성 단각류인 M. uenoi의 생식 능력에 미치는 장기적 영향을 평가하였다. 급성 노출(96시간) 실험에서는 유의미한 생존율 감소가 관찰되지 않았으나, 28일 이상의 만성 노출 실험에서는 세대가 거듭될수록 생식력이 치명적으로 저하되는 결과를 확인하였다. 이는 미세플라스틱이 단기적인 생존에는 영향을 미치지 않더라도, 장기적으로는 개체군의 유지에 필수적인 생식 과정에 심각한 교란을 유발할 수 있음을 시사한다(Fig. 4).
이러한 결과는 퇴적물 내 미세플라스틱 노출이 저서무척추동물에 미치는 부정적 영향을 보고한 선행연구들과 일치한다. Green[2016], Green et al.[2019]은 PVC(폴리염화 비닐, Polyvinyl Chloride) 및 PLA(폴리젖산, polylactic acid)와 같은 미세플라스틱이 갯지렁이(Arenicola marina)의 섭식 및 굴착 행동을 저해하여 생물량을 감소시킨다고 보고하였으며, 이는 서식지 생태계의 기능 저하로 이어질 수 있음을 보여준다. 또한, Ziajahromi et al.[2018]은 담수 곤충 깔따구(Chironomus tepperi) 유충이 PE(폴리에틸렌, polyethylene) 미세플라스틱에 노출되었을 때 생존율과 우화율이 현저히 감소함을 확인하여, 미세플라스틱이 생물의 초기 발달 및 생식 단계에 결정적 영향을 미칠 수 있음을 규명하였다.
본 연구에서 특히 주목할 점은 암컷의 노출이 생식 실패에 결정적인 역할을 했다는 것이다. 암수 모두 노출된 그룹과 암컷만 노출된 그룹에서 자손 생산이 완전히 억제된 반면, 수컷만 노출된 그룹에서는 미미하게나마 자손이 생산되었다(Fig. 5, Table 3 참조). 이는 미세플라스틱 또는 관련 유해 물질이 난자 형성, 난황 축적, 산란 등 암컷의 내분비계 생식 과정에 직접적인 교란을 일으켰을 가능성을 강하게 시사한다. 이러한 결과는 Sussarellu et al.[2016]이 굴에서 확인한 생식력 저하 및 Ye et al.[2025]이 제브라피쉬에서 보고한 내분비계 교란 연구 결과와 그 맥락을 같이하며, PET 미세플라스틱이 체내에 물리적으로 축적되어 생리적 장애를 유발함을 뒷받침한다.
더 나아가, 본 연구는 미세플라스틱의 영향이 세대를 거쳐 누적되고 증폭될 수 있음을 명확히 보여주었다. F1의 생식력이 대조군 대비 약 50% 수준으로 감소했으며, F2에서는 제한적인 생식 기능만 유지되었고 F3은 거의 출현하지 않았다. 이는 생존율이 높게 유지되더라도 세대 간 생식 실패가 누적되어 결국 개체군 붕괴로 이어질 수 있음을 의미한다. Zhao et al.[2023]은 해양 요각류에서 나노플라스틱이 후성유전학적 변형(DNA 메틸화)을 통해 여러 세대에 걸쳐 생식 기능을 완전히 상실시키는 것을 보고하였는데, 본 연구에서 관찰된 F3 출현 실패 현상 또한 유사한 기작에 의한 '세대 간 생식 연속성(reproductive continuity)'의 단절로 해석될 수 있다.
이러한 강력한 생식 독성의 기저에는 실험에 사용된 마이크로미터(μm) 수준의 플라스틱에 혼재했을 가능성이 있는 나노미터(nm) 크기 입자의 영향이 있었을 것으로 추정된다. 나노플라스틱은 크기가 작아 세포막 투과성이 높고, 이로 인한 세포 내 축적, 활성산소(ROS) 생성, DNA 손상 등 마이크로플라스틱보다 훨씬 높은 수준의 세포 독성을 유발할 수 있다(Waldschlager et al.[2022]). 특히 Płuciennik et al.[2024]은 나노 입자가 유도하는 활성산소가 p53 단백질을 활성화시켜 세포주기를 정지시키거나 세포 사멸(apoptosis)을 유도한다고 보고하였는데, 이러한 기작은 생식세포나 배아 세포에 치명적인 손상을 주어 본 연구에서 관찰된 생식 실패 및 세대 단절 현상을 생물학적으로 설명하는 강력한 근거가 된다.
5. 결 론
본 연구는 퇴적물 기반 PET 미세플라스틱이 단순한 물리적 이물질을 넘어 저서생물의 생식 기능에 직접적인 화학·생리적 교란을 일으키는 유해 물질임을 실증하였다. 특히, 대부분의 선행 연구가 단기적 생존율에 초점을 맞춘 급성독성 평가에 머무른 반면, 본 연구는 장기적인 만성 노출, 특히 여러 세대에 걸친 생식독성을 직접적으로 규명했다는 점에서 학술적 의의가 있다. 급성 노출에서는 뚜렷한 영향이 없었으나 만성 노출 조건에서 생식 기능이 완전히 마비되는 현상은 미세플라스틱의 실질적 위협이 ‘생존’이 아닌 ‘종의 존속’ 자체를 위협하는 아급성 영향(sub-lethal effect)에 있음을 명백히 보여준다.
더 나아가 1, 2세대 연속 노출 이후 3세대의 출현이 완전히 억제되는 결과는, 독성이 단일 개체에서 끝나지 않고 세대를 거쳐 누적·증폭되어 결국 개체군 붕괴로 이어질 수 있다는 ‘세대 간 독성(transgenerational toxicity)’이라는 새로운 차원의 위험을 명확히 제시한다. 이는 미세플라스틱의 생태계 위해성을 평가하고 관련 환경 기준을 마련할 때, 단기적인 급성독성 평가만으로는 그 위험성을 심각하게 과소평가할 수 있음을 경고하는 강력한 증거가 될 수 있다.
따라서 향후 해양 저서 생태계 보호를 위해서는 개체군의 유지에 필수적인 생식력과 세대 간 영향을 핵심 평가 지표로 포함하는 장기적인 관점의 연구와 정책적 접근이 요구된다.
Acknowledgments
본 연구는 2025년도 해양수산부 재원, 해양수산과학기술진흥원-해양생태계 보호기준 마련을 위한 위해성평가 사업의 지원을 받아 수행하였습니다(KS221614).
References
-
Aramendia, J., Garcia-Velasco, N., Amigo, J.M., Izagirre, U., Seifert, A., Soto, M. and Castro, K., 2024, Evidence of internalized microplastics in mussel tissues detected by volumetric Raman imaging. Sci. Total Environ., 914, 169960.
[https://doi.org/10.1016/j.scitotenv.2024.169960]

- Barboza, L.G.A., Lopes, C., Oliveira, P., Bessa, F., Otero, V., Henriques, B. and Guilhermino, L., 2020, Environmental toxicology of microplastics on fish: A review. Environmental Pollution, 267, 115643.
-
Browne, M.A., Dissanayake, A., Galloway, T.S., Lowe, D.M. and Thompson, R.C., 2008, Ingested microscopic plastic translocates to the circulatory system of the mussel, Mytilus edulis (L.). Environ. Sci. Technol., 42(13), 5026-5031.
[https://doi.org/10.1021/es800249a]

-
Calmão, M., Nogueira, S.T.O., Rodrigues, M.F.S., Novais, S.C., Pereira, J.L., Soares, A.M.V.M., da Fonseca, V.B.S.S.M. and Freitas, R., 2023, Time-course distribution of fluorescent microplastics in target tissues of mussels and polychaetes. Chemosphere, 311(2023), 137087.
[https://doi.org/10.1016/j.chemosphere.2022.137087]

-
Chae, Y., Heo, Y., Choi, J.S., Nam, H., Kim, T.H. and Park, J.-W., 2025, Kinetics and toxicity of atypical microplastics in the manila clam Ruditapes philippinarum: A quantitative analysis of accumulation and excretion. Reg. Stud. Mar. Sci., 82, 104012.
[https://doi.org/10.1016/j.rsma.2025.104012]

-
Coady, K.K., Ankley, G.T., Berninger, J.P., Biales, A.D., de la Barrera, B., Denny, J.S., Embry, M.R., Franzosa, J.A., Gulledge, M.F., LaRocca, C.A., Stahl, T. and Vogs, C., 2017, Current limitations and recommendations to improve testing for endocrine active substances. Integr. Environ. Assess. Manag., 13(2), 302-316.
[https://doi.org/10.1002/ieam.1862]

- da Costa Araújo, A.P., Malafaia, G. and Paiva, R., 2020, Microplastic ingestion by fish: A review. Sci. Total Environ., 746, 140217.
-
da Costa Araújo, A.P. and Malafaia, G., 2021, Microplastic ingestion induces behavioral disorders in mice: A preliminary study on the trophic transfer effects via tadpoles and fish. J. Hazard. Mater., 401, 123263.
[https://doi.org/10.1016/j.jhazmat.2020.123263]

-
Duncan, E.M., Broderick, A.C., Fuller, W.J., Galloway, T.S., Godfrey, M.H., Hamann, M., Limpus, C.J., Lindeque, P.K., Mayes, A.G., Omeyer, L.C.M., Santillo, D., Snape, R.T.E. and Godley, B.J., 2019, Microplastic ingestion ubiquitous in marine turtles. Glob. Change Biol., 25(2), 744-752.
[https://doi.org/10.1111/gcb.14519]

- GESAMP, 2015, Sources, fate and effects of microplastics in the marine environment: a global assessment. In: Kershaw, P. J. (Ed.), IMO/FAO/UNESCO-IOC/UNIDO/WMO/IAEA/UN/UNEP/UNDP Joint Group of Experts on the Scientific Aspects of Marine Environmental Protection, Rep. Stud. GESAMP No. 90, 96 p.
- Green, D.S., 2016, Effects of microplastic exposure on the body condition and behaviour of planktivorous fish. Environ. Pollut., 211, 240-247.
- Green, D.S., Boots, B., Blockley, D.J., Rocha, C. and Thompson, R., 2019, Sediment contamination by microplastics and its implications for benthic organisms. Environ. Sci. Technol., 53(4), 2033-2043.
-
Hermabessiere, L., Dehaut, A., Paul-Pont, I., Lacroix, C., Jezequel, R., Soudant, P. and Duflos, G., 2017, Occurrence and effects of plastic additives on marine environments and organisms: a review. Chemosphere, 182, 781-793.
[https://doi.org/10.1016/j.chemosphere.2017.05.096]

-
Hu, L., Chernick, M., Hinton, D.E. and Shi, H., 2018, Microplastics in small waterbodies and tadpoles from the Yangtze River Delta, China. Environ. Sci. Technol., 52(15), 8885-8893.
[https://doi.org/10.1021/acs.est.8b02279]

- Jeong, C.-B., Won, E.-J., Kang, H.-M., Lee, M.-C., Hwang, D.-S., Hwang, U.-K., Zhou, B., Souissi, S., Lee, S.-J. and Lee, J.-S., 2020, Effects of microplastics exposure on ingestion, fecundity, development, and dimethylsulfide production in Tigriopus japonicus. Environ. Sci. Technol., 54(2), 1037-1045.
-
Jovanović, B., 2017, Ingestion of microplastics by fish and its potential consequences from a physical perspective. Integr. Environ. Assess. Manag., 13(3), 510-515.
[https://doi.org/10.1002/ieam.1913]

-
Kühn, S., Bravo Rebolledo, E.L. and van Franeker, J.A., 2015, Deleterious effects of litter on marine life, in: Bergmann, M., Gutow, L., & Klages, M. (Eds.), Marine Anthropogenic Litter, Springer, 75-116.
[https://doi.org/10.1007/978-3-319-16510-3_4]

-
McNeish, R.E., Kim, L.H., Barrett, H.A., Mason, S.A., Kelly, J.J. and Hoellein, T.J., 2018, Microplastic in riverine fish is connected to species traits. Sci. Rep., 8, 11639.
[https://doi.org/10.1038/s41598-018-29980-9]

- National Institute of Fisheries Science, 2023, Marine Environmental Official Test Standards (Notification No. 2023-12). Republic of Korea: Ministry of Oceans and Fisheries.
- Nelms, S.E., Duncan, E.M., Broderick, A.C., Galloway, T.S., Godfrey, M.H., Hamann, M., Lindeque, P.K. and Godley, B.J., 2019, Plastic and seabirds: Coral celebrates consumption. Environ. Pollut., 247, 59-66.
-
Płuciennik, K., Sicińska, P., Misztal, W. and Bukowska, B., 2024, Important Factors Affecting Induction of Cell Death, Oxidative Stress and DNA Damage by Nano- and Microplastic Particles In Vitro. Cells, 13(9), 768.
[https://doi.org/10.3390/cells13090768]

-
Sussarellu, R., Suquet, M., Thomas, Y., Lambert, C., Fabioux, C., Pernet, M.E.J., Le Goic, N., Quillien, V., Mingant, C., Epelboin, Y., Corporeau, C., Guyomarch, J., Robbens, J., Paul-Pont, I., Soudant, P. and Huvet, A., 2016, Oyster reproduction is affected by exposure to polystyrene microplastics. Proc. Natl. Acad. Sci. U.S.A., 113(9), 2430-2435.
[https://doi.org/10.1073/pnas.1519019113]

- U.S. Environmental Protection Agency., 2001, Methods for Assessing the Chronic Toxicity of Marine and Estuarine Sediment-associated Contaminants with the Amphipod Leptocheirus plumulosus (EPA/600/R-01/020), Office of Research and Development Washington, DC 20460.
-
von Moos, N., Burkhardt-Holm, P. and Kohler, A., 2012, Uptake and effects of microplastics on cells and tissue of the blue mussel Mytilus edulis L. after an experimental exposure. Environ. Sci. Technol., 46(20), 11327-11335.
[https://doi.org/10.1021/es302332w]

-
Waldschläger, K., Brückner, M.Z.M., Carney Almroth, B., Hackney, C.R., Adyel, T.M., Alimi, O.S., Belontz, S.L., Cowger, W., Doyle, D., Gray, A., Kane, I., Kooi, M., Kramer, M., Lechthaler, S., Michie, L., Nordam, T., Pohl, F., Russell, C., Thit, A. and Wu, N., 2022, Learning from natural sediments to tackle microplastics challenges: A multidisciplinary perspective. Earth-Sci. Rev., 228, 104021.
[https://doi.org/10.1016/j.earscirev.2022.104021]

- Wang, J., Liu, X., Li, Y., Powell, T., Wang, X., Wang, G. and Zhang, P., 2021, Microplastics as contaminants in the soil environment: A mini-review. Sci. Total Environ., 790, 148156.
-
Windsor, F.M., Tilley, R.M., Tyler, C.R. and Ormerod, S.J., 2019, Microplastic ingestion by riverine macroinvertebrates. Sci. Total Environ., 646, 68-74.
[https://doi.org/10.1016/j.scitotenv.2018.07.271]

-
Ye, J., Zhang, X., Cui, Y., Wu, Z. and Li, Z., 2025, Synergistic endocrine disruption and cellular toxicity of polyethylene microplastics and bisphenol A in MLTC-1 cells and zebrafish. Sci. Rep., 15(1), 3412.
[https://doi.org/10.1038/s41598-025-94902-5]

- Zhao, F., Wang, Q., Wang, Z. and Li, Y., 2023, Nanoplastics induce epigenetic signatures of transgenerational reproductive toxicity in marine copepods under ocean acidification. Sci. Total Environ., 868, 162698.
- Ziajahromi, S., Kumar, A., Neale, P.A. and Leusch, F.D.L., 2018, Impact of microplastic contamination on the growth and emergence of a freshwater insect. Environ. Pollut., 236, 652-661.
