2000-2024년 여수 해역의 Margalefidinium polykrikoides에 의한 유해성 적조 발생 특성: 영양염류 농도 및 비율을 중심으로
초록
식물플랑크톤은 해양 1차 생산의 50% 이상을 담당하며, 지구 탄소순환과 해양 먹이망의 기초를 이루는 핵심 생물군이다. 그러나 환경 요인의 변화로 특정 유해성 종이 대량 증식하면 적조가 발생하여 해양 생태계 교란, 수산업 피해, 인체 건강 위험 등 심각한 문제를 초래한다. 따라서 어떤 환경 조건에서 유해성 적조종이 대규모로 발생하는지를 규명하고 이를 예측하는 것은 어업에 종사하는 우리나라 국민의 피해를 최소화하기 위해 매우 중요하다. 본 연구는 해양환경측정망과 국립수산과학원 적조 속보에 장기간 축적된 데이터 중, 2000~2024년 25년간의 자료를 활용하여, 한국 남해안에서 주요 유해성 적조 원인 종의 대규모 발생 메커니즘을 분석하였다. 연구 결과, 지난 25년간 우리나라 해역에서 Margalefidinium polykrikoides (= Cochlodinium polykrikoides)에 의한 적조가 가장 많이 발생(435회)하였으며, 이 종에 의한 적조는 8월 여수 해역에서 가장 많이 발생한 것으로 밝혀졌다. 또한, M. polykrikoides의 개체수가 가장 높았던 2001년, 2015년, 2013년 8월의 영양염류 조건을 분석한 결과, 표층의 N:P 비는 4.8 미만, 저층의 N:P 비는 3.8 미만으로 매우 낮은 비율을 보였으며, 우리나라 여수 해역에서 N:P 비가 낮을 때 M. polykrikoides에 의한 대규모 적조가 발생하였다는 사실을 새롭게 규명하였다. 또한, 질산염의 저층-표층 농도 차이가 0에 가까울수록 적조가 더 많이 발생하는 경향을 처음으로 확인하였다. 본 연구 결과는 질소가 고갈되고 규산염이 풍부한 환경에서 M. polykrikoides의 대규모 적조가 집중적으로 발생한다는 점을 보여주며, 이는 영양염 농도와 비율의 복합적 변화가 적조 발생을 유발하는 주요 조절 요인임을 시사한다. 또한 저층과 표층의 용존무기인산염 농도 차가 커질수록 M. polykrikoides에 의한 대규모 적조가 발생함을 밝혔다. 따라서 향후 여수 해역의 저층 인산염 농도가 지속적으로 증가하고, 저층과 표층의 질산염 및 규산염의 불균형이 심화될 경우, M. polykrikoides 적조가 더욱 빈번하고 심화될 가능성을 보여주며, 이에 따라 영양염 농도 변화 및 비율과 적조 발생에 대한 지속적인 모니터링의 필요성을 강조한다. 이러한 발견은 향후 적조 예측 모델의 정확도를 높이고, 효과적인 대응 전략을 수립하는 데 중요한 학문적, 사회적 기반을 마련할 것으로 기대된다.
Abstract
Phytoplankton contribute more than 50% of marine primary production and form the foundation of global carbon cycling and marine food webs. However, when certain harmful species proliferate massively under changing environmental conditions, red tides occur, causing serious problems such as disruption of marine ecosystems, damage to fisheries, and risks to human health. Therefore, identifying the environmental conditions under which harmful algal species form large-scale blooms, and predicting their occurrence, is crucial to minimizing the impacts on fisheries-dependent communities in Korea. This study analyzed the bloom mechanisms of major harmful algal species in the southern coastal waters of Korea using 25 years (2000–2024) of long-term data accumulated from the Marine Environment Monitoring Network and the harmful algal bloom (HAB) alert system of the National Institute of Fisheries Science, Korea. The results showed that Margalefidinium polykrikoides (= Cochlodinium polykrikoides) was the most frequent bloom-forming species, with 435 recorded events over the past 25 years, and that its blooms occurred most frequently in August in the Yeosu region. Nutrient conditions during the peak bloom years of 2001, 2015, and 2013 revealed extremely low N:P ratios, with surface values below 4.8 and bottom values below 3.8, indicating that large-scale M. polykrikoides blooms were associated with low N:P environments. In addition, we newly confirmed that the closer the nitrate concentration difference between surface and bottom waters approached zero, the more frequently blooms occurred. Furthermore, the results demonstrated that large-scale blooms of M. polykrikoides were concentrated under nitrogen-depleted and silicate-rich conditions, suggesting that the combined variation in nutrient concentrations and stoichiometric ratios (N:P:Si) acts as a key regulatory driver of bloom development. It was also revealed that large-scale red tides caused by M. polykrikoides occur more frequently as the difference in dissolved inorganic phosphate concentration between the bottom and surface layers increases. This implies that if bottom-water phosphate concentrations continue to rise and the imbalance of nitrate and silicate between surface and bottom waters intensifies, the frequency and magnitude of M. polykrikoides blooms in the Yeosu coastal region are likely to increase. These results indicate a potential causal link between changes in nutrient structure and bloom formation, highlighting the importance of continuous and integrated monitoring of nutrient concentrations and ratios to better predict bloom dynamics. These findings provide novel evidence of the key environmental conditions driving M. polykrikoides blooms, and are expected to enhance the accuracy of future bloom prediction models while establishing an essential academic and societal basis for effective management strategies.
Keywords:
Cochlodinium polykrikoides, Red tide, Marine ecosystem, Nutrients, N:P ratio키워드:
코클로디니움 폴리크리코이데스, 적조, 해양 생태계, 영양염, 질소:인 비1. 서 론
식물 플랑크톤은 해양에서 50% 이상의 글로벌 1차 생산과 대기 중 이산화탄소 흡수 및 산소 공급을 담당하는 지구 생태계의 핵심 구성원으로, 해양 먹이그물의 기초와 탄소순환 중심에 있다(Baumert and Petzoldt[2008]; Falkowski et al.[1998]; Field et al.[1998]). 식물플랑크톤은 규조류(diatoms), 와편모류(dinoflagellates), 남세균류(cyanobacteria) 등 다양한 분류군으로 구성되어 있으며, 각 군은 해양 생태계에서 다양한 역할을 담당한다(Anderson et al.[2021]; Sun et al.[2022]). 하지만 이들이 영양염, 수온, 광, 수괴 안정도 등의 환경 변화로 인해 대량 번식할 경우 적조(red tide) 또는 유해성 조류 대번성(harmful algal bloom, HAB)이 발생하며, 해양생물 대량 폐사, 해양생태계 교란, 어업 및 인체 건강에 부정적 영향을 초래한다(Anderson et al.[2012]; Rolton et al.[2022]).
적조는 어업 및 양식 산업, 해양생태계, 인간 건강에 심각한 위협을 초래하는 글로벌 해양 환경 문제로 인정받고 있으며, 전 세계적으로 수산생물의 대량 폐사, 산소 고갈, 미생물 및 독성 미량원소 증가, 식중독이나 패류독소 등 인체 건강에 대한 직접적 위험 및 관광, 어업 경제 위축을 유발한다(Berdalet et al.[2015]; Hoagland and Scatasta[2006]; Lenzen and Murray[2021]). Margalefidinium polykrikoides(= Cochlodinium polykrikoides)는 온대 및 열대 해역에서 빈번하게 유해성 적조를 일으키는 대표적 와편모류로, 한국, 라틴 아메리카, 호주 등 전 세계 주요 해역에서 반복적으로 대규모 적조를 일으켜왔다(López-Cortes et al.[2019]; Griffith et al.[2019]; Park et al.[2019]). 이 종은 점액(mucus)을 분비하여 높은 세포 응집력을 가지고 있어, 고밀도 분포 시 어류 아가미에 붙어 호흡 기능을 저해하며 단시간 내 집단 폐사를 유발한다(Dorantes-Aranda et al.[2010]; de Silva and Gobler.[2023]; Kim et al.[2000]).
한국 남해안에서 M. polykrikoides는 최근 30여 년간 연평균 10~30건 내외의 적조 발생을 기록하며 특히 남해안 어류 대량 폐사의 가장 큰 원인종으로 꼽힌다(Shin et al.[2021]). 1995년 남해안에서는 최대 30,000 cells/mL의 M. polykrikoides bloom이 46일 이상 지속되면서 양식 어류의 10% 이상이 폐사하였고, 이로 인한 경제적 손실은 약 6,000만 달러에 달했다(Park et al.[2013]). 또한 1991~2012년 누적 피해액이 약 1억 2,100만 달러에 이르며, 대규모 적조와 어업 피해는 남해안을 중심으로 광범위하게 반복 발생하였다(Park et al.[2013]). 이처럼 M. polykrikoides는 단일 종으로 국내외 해양생태계와 어업에 가장 많은 피해를 유발하는 종 중 하나이며, 대형 적조 발생 예측 및 메커니즘 규명은 해양 환경 및 어업 관리에서 가장 중요한 현안으로 인식되고 있다(Griffith et al.[2023]; Hofmann et al.[2021]).
M. polykrikoides는 N, P, Si 등 영양염의 농도가 낮은 환경에서도 잘 생존하며, 수온이 15~30℃, 염분이 20~36 psu일 때 대량 증식하는 경향이 있다(Hofmann et al.[2021]; Kim et al.[2004]). 또한 혼합영양(mixotrophy)을 활용하여 식물성 플랑크톤, 박테리아, 유기영양염 등 다양한 유기 입자를 섭식할 수 있으며, 일주기 수직 이동(diel vertical migration)을 통해 빛과 영양분이 풍부한 최적 수층으로 이동한다(Clayton et al.[2024]; Lim et al.[2022]). 특히 일주기 수직이동 과정에서 밤에 보다 깊은 수층의 무기 및 유기 영양원을 이용하고, 주간에는 표층에서 광합성을 수행하여 에너지와 영양분을 효율적으로 최대화한다(Clayton et al.[2024]; Lim et al.[2022]). 이러한 생태생리학적 특성으로 인해 M. polykrikoides가 다양한 해양 환경에서 적조를 형성하고 빠르게 확산되며, 반복적인 피해가 발생할 수 있으므로 적조 메커니즘의 이해와 관리가 매우 절실하다.
지금까지의 연구는 수온, 염분, 총 질소 및 인 등 환경 요인과 적조 발생 시기, 분포 간 연관성에 초점을 맞추었으나, 실제 현장 기반 데이터에서 질소(N), 인(P), 규소(Si)의 상대적 비(N:P:Si)와 표층-저층 구배 등 입체적 요인이 적조 발생에 미치는 영향은 거의 밝혀지지 않았다(Carney-Almeida et al.[2024]; Kim et al.[2023]; Park et al.[2019]; Pérez-Vega et al.[2025]). 따라서 본 연구는 2000년부터 2024년까지 25년간 여수 연안에서 8월에 수집된 장기 관측 자료를 기반으로, 표층 및 저층의 환경 요인과 M. polykrikoides 개체수 간의 상관관계를 분석하였다. 특히 영양염 농도뿐만 아니라 N:P 및 N:P:Si 비율과 층별 영양염 분포 차이를 함께 고려함으로써 적조 발생 메커니즘에 대한 새로운 통찰을 제공하고자 한다. 본 연구의 결과는 향후 적조 예측 모델 개발과 효과적인 대응 전략 수립에 기여할 수 있을 것으로 기대된다.
2. 자료 및 방법
2.1 자료 수집
본 연구에서는 2000년부터 2024년까지의 국립수산과학원에서 제공하는 적조 속보 자료(https://www.nifs.go.kr)와 해양환경공단의 해양환경측정망 수질 자료(https://www.meis.go.kr)를 활용하였다. 먼저 국립수산과학원의 적조 속보 자료를 2000년부터 2024년까지의 기간에 걸쳐 수집하여, 발생 보고된 모든 적조 종의 출현 빈도를 정리하였다. 이를 바탕으로 연구 기간 동안 국내 연안에서 가장 빈번하게 적조를 일으킨 종을 선정하였으며, 해당 종의 적조가 가장 자주 발생한 지역과 시기를 교차 분석을 통해 도출하였다.
이후 해양환경측정망 자료 중, 선정된 주요 발생 해역과 시기를 대표할 수 있는 정점을 탐색하였고, CK2401, CK2402 정점을 대규모 적조 발생과 공간적으로 가장 밀접하게 연관되는 지점으로 선정하였다. CK2401는 북위 34°41'26", 동경 127°50'42"이고 CK2402는 북위 34°37'12", 동경 127°48'25"이며, 두 정점에서 2000~2024년 동안 8월에 수집된 수질 및 환경 자료를 연구 대상으로 활용하였다(Fig. 1).
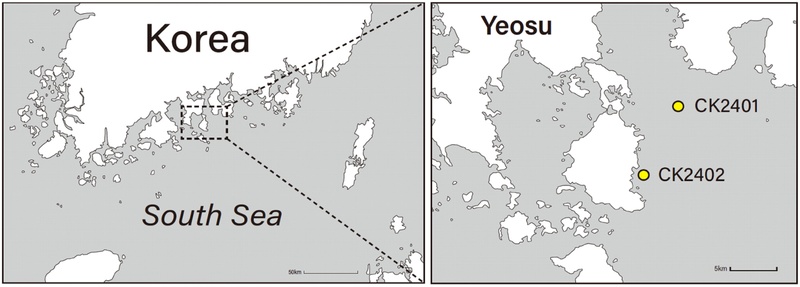
Monitoring stations of the Marine Environmental Monitoring Network operated by Korea Marine Environment Management Corporation (KOEM) in the Yeosu coastal area.
분석된 환경 요인은 수온, 염분, DO, 영양염(ammonium, NH4; nitrite, NO2; nitrate, NO3; dissolved inorganic nitrogen, DIN; total nitrogen, TN; dissolved inorganic phosphorus, DIP; total phosphorus, TP; silicate, SiO2), SS(suspended solid), Chl-a(chlorophyll-a), 투명도 등으로, 표층과 저층 자료를 모두 포함하였다. 저층 데이터는 해저 바닥으로부터 최대 1 m 이내의 수층 관측 자료이다. 각 항목은 CK2401과 CK2402 정점의 평균값을 산출하여 적조 발생 지역의 대푯값으로 사용하였으며, 환경 요인 데이터를 μM 단위로 환산하여 분석하였다. 또한 저층-표층 간 차이를 산출하여 수직 농도 차를 계산하였다. DIN은 NH4, NO2, NO3의 합으로 계산하였으며, DIP와 규산염은 각각 PO4와 SiO2 값으로부터 환산하였다. 이를 바탕으로 DIN:PO4 비(N:P) 및 DIN:SiO2 비(N:Si)를 계산하였다.
2.2 통계 분석
통계분석은 연도별 환경요인의 장기적 변화를 확인하기 위해 단순 선형회귀분석을 수행하였으며, M. polykrikoides 최대 개체수와 환경요인 간의 관계는 피어슨 상관분석을 통해 검토하였다. 통계적 유의수준은 p=0.05로 설정하였다. 추가적으로, 연도별 및 조건별 환경요인의 차이를 검정하기 위해 일원배치 분산분석(one-way analysis of variance)을 적용하였으나, 정규성 및 등분산성 조건이 충족되지 않아 비모수 검정인 Kruskal-Wallis test를 사용하여 보완 분석을 진행하였다.
통계 분석은 R Studio(Version 4.5.1)에서 수행하였으며, Microsoft Excel은 자료 처리, 기초 통계 계산과 보조적 시각화에 활용하였다. 그래프는 연도별 추세를 나타내는 선형 회귀선, 발생 일수와 최대 개체수를 나타내는 막대그래프, 환경요인과의 관계를 나타내는 산점도로 구성하였다.
3. 결과 및 고찰
3.1 적조의 주요 발생 현황과 공간적 분포
2000~2024년 장기 자료 분석 결과, 적조를 가장 빈번하게 일으킨 종은 M. polykrikoides로 총 435회 발생하였으며, Heterosigma akashiwo(82회), Ceratium furca(65회), Akashiwo sanguinea(53회)보다 압도적으로 높은 수치를 보였다(Fig. 2a). 특히 M. polykrikoides의 발생 횟수는 두 번째로 빈도가 높은 Heterosigma akashiwo 대비 약 5배 이상 높아, 본 종이 한국 연안 적조의 주된 원인종임을 확인할 수 있었다. 이러한 양상은 1990년대 이후 국내 해역에서 M. polykrikoides가 가장 우점적인 적조종으로 자리 잡았음을 보고한 기존 연구와 부합한다(Lee et al.[2013]; Lim et al.[2020]).
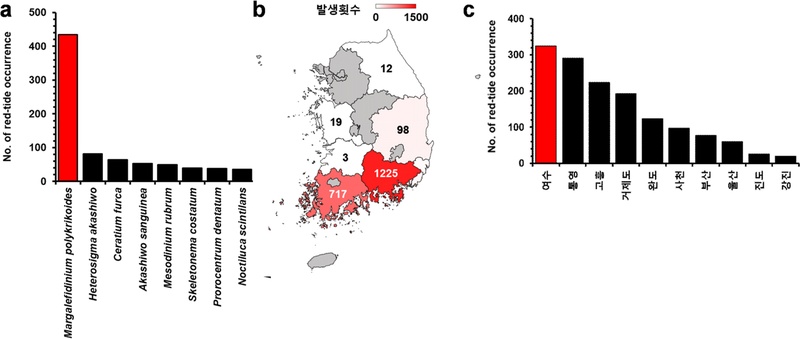
(a) Number of red tide occurrences by causative species in Korean coastal waters. (b) Number of red tide events by province. (c) Number of red tide events by region.
M. polykrikoides 적조는 경상남도에서 1,225회로 가장 많이 발생하였으며, 전라남도에서 717회, 경상북도에서는 98회 발생하였다(Fig. 2b). 또한 여수 연안에서 324회로 단일 지역 중 최다 발생을 기록하였으며, 통영(291회), 고흥(224회), 거제도(193회) 순으로 높은 빈도를 나타냈다(Fig. 2c). 이는 남해 중부와 남해 동부 연안을 중심으로 적조가 발생하였음을 시사하며, 여수, 통영, 남해 일대에서 반복적인 대규모 발생을 보고한 기존 연구들과도 일관된 경향을 보였다(Gyoon et al.[2001]; Yang et al.[2024]).
3.2 8월 M. polykrikoides 적조 발생 일수와 최대 개체수의 연도별 변화
적조가 가장 많이 발생한 8월 한 달 동안 여수 지역에서 M. polykrikoides 적조가 관측된 일수를 연도별로 집계한 결과, 2015년에 21일로 조사 기간 중 최장 발생 기간을 기록하였다(Fig. 3a). 2012년과 2013년에도 18일로 적조가 비교적 장기간 지속되었다. 반면, 2005년, 2008년, 2009년, 2010년, 2011년, 2017년, 2020년, 2023년에는 8월 중 적조 발생이 전혀 보고되지 않았으며, 2001년, 2002년, 2003년, 2004년, 2006년, 2007년, 2021년에는 1일만 발생한 것으로 보고되었다.
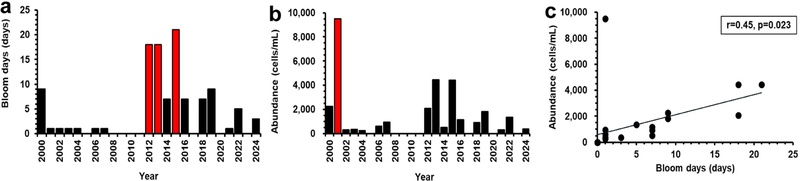
Interannual variation of red-tide occurrences by Margalefidinium polykrikoides in August in waters off Yeosu (a) Number of days in August with observed red tide occurrences. (b) Maximum cell density (cells/mL) recorded in August. (c) Correlation between the number of occurrence days and the maximum cell density.
8월의연도별최대개체수를 비교한결과, 2001년에 9,500 cells/mL로 가장 높은 값을 기록하였다(Fig. 3b). 그 뒤로 2013년(4,441 cells/mL), 2015년(4,434 cells/mL), 2000년(2,254 cells/mL) 순이었다. 대부분의 연도(2002~2011, 2014, 2017, 2018, 2020, 2021, 2023, 2024)에서는 최대 개체수가 1,000 cells/mL 이하로 낮았다.
적조 발생 일수와 최대 개체수 간의 상관분석을 한 결과, 유의미한 양의 상관관계가 확인되었다(r=0.45, p=0.023)(Fig. 3c). 이는 적조의 장기화가 개체수 증가와 연관될 수 있음을 시사하며, 장기적인 출현 빈도가 고밀도 발생으로 이어질 수 있다는 잠재성을 보여준다. 이러한 결과는 적조의 지속 시간과 강도가 밀접하게 연관된다는 기존 연구와 일치한다(Lee[2008]; Lee et al.[2023]). 2001년에 적조 발생이 1일로 기록되었지만, 가장 높은 개체수를 보였는데, 이는 당시 영양염 조건이 제한적이었거나, 미생물 군집 및 저서 생물군에 의한 생물학적 제어 요인이 작용했을 가능성을 보여준다(Kim et al.[2010]; Lee[2006]). 즉, 적조의 발생 일수는 군집의 지속가능성을 반영하는 지표이지만, 영양염 공급이나 수온 등의 외부 요인에 따라 실제 최대 개체수는 달라질 수 있다.
3.3 장기적 영양염 농도 변화와 수직 농도차 추세
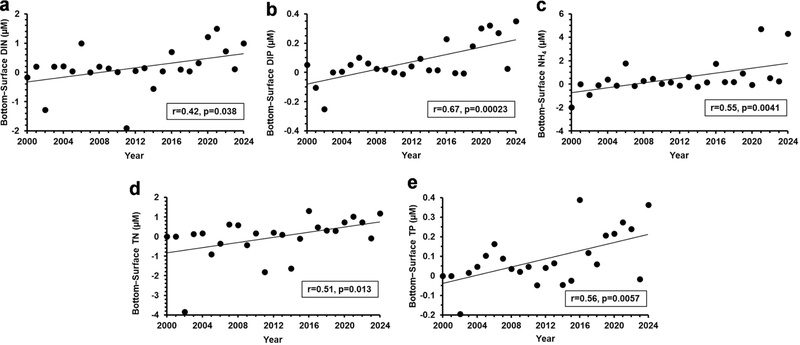
2000~2024년 동안 여수지역의 8월 표층 영양염 농도 변화를 분석한 결과, DIN 농도는연도에따라유의미한경향이없었으나(r = -0.38, p = 0.065), DIP, NH4, TN, TP 농도는 연도에 따라 유의하게 감소하였다(DIP: r = -0.54, p = 0.0057; NH4: r = -0.54, p = 0.0056; TN: r = -0.54, p = 0.0074; TP: r = -0.51, p = 0.014)(Fig. 4). 이는 장기적으로 표층에서 이용 가능한 영양염이 점차 고갈되고 있음을 시사하며, 특히 여름철 표층에서 영양염 제한이 심화되고 있음을 보여준다. 반면, DIN, DIP, NH4, TN, TP의 저층-표층 농도 차는 모두 유의미한 증가 경향을 나타냈다(DIN: r = 0.42, p = 0.038; DIP: r = 0.67, p = 0.00023; NH4: r = 0.55, p = 0.0041; TN: r = 0.51, p = 0.013; TP: r = 0.56, p = 0.0057)(Fig. 5). 특히 시간 변화에 따라 여수 해역의 DIP의 저층과 표층 간 농도 차이가 점점 증가하는 것을 관찰할 수 있었다(Fig. 5b, 5e). 이러한 현상은 기후변화에 따른 해양 성층 강화, 하계 담수 유입에 따른 혼합 저하, 부영양화 이후의 장기적 탈질화와 같은 복합적 요인에 의해 설명된다(Anderson et al.[2002]; Heisler et al.[2008]; Lee[2006]). 또한, 2000년대 이후 남해 연안에서 진행된 하수처리시설 확충, 총오염부하관리제 (TPLMS; Total Pollution Load Management System) 도입, 비점오염원 관리 강화, 농업용 비료 사용량 감소 등 인위적 수질관리 조치가 표층으로의 영양염 유입량을 저감시켜, 영양염 농도의 장기적 감소에 기여한 것으로 판단된다(Chang et al.[2012]; Park et al.[2018]).
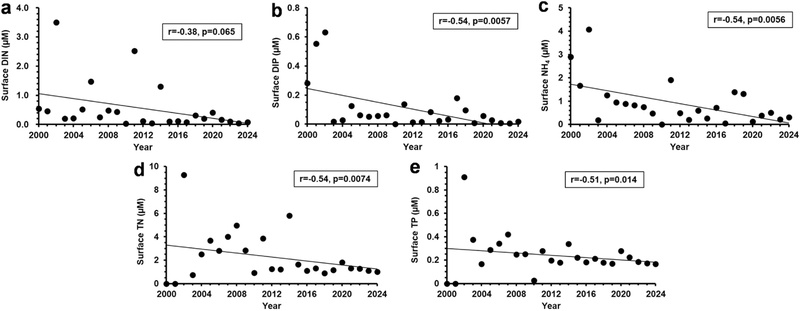
Temporal trends in surface nutrient concentrations in August from 2000 to 2024. (a) dissolved inorganic nitrogen (DIN), (b) dissolved inorganic phosphorus (DIP), (c) ammonium (NH4), (d) total nitrogen (TN), and (e) total phosphorus (TP).
3.4 환경요인과 개체수 간의 관계
본 연구에서는 M. polykrikoides가 특정 영양염류 환경에서 적조를 강하게 일으키는 양상을 규명하기 위해, 8월 여수 해역에서 N:P 및 N:Si 비율에 따른 M. polykrikoides의 밀도를 분석하였다. 연구 결과, M. polykrikoides 적조가 낮은 N:P 비 환경에서 높은 밀도로 발생하는 경향을 보였다. 표층 N:P 비는 16 미만인 환경에서 개체수가 높았으며, N:P 비가 낮아질수록 개체수가 증가하였다(Fig. 6a). 저층 N:P 비에서도 동일한 경향이 나타났으며, 16 미만 구간에서 개체수가 두드러지게 증가하였다(Fig. 6b). 특히, 지난 25년간 M. polykrikoides의 개체수가 가장 높았던 2001년, 2015년, 2013년의 표층의 N:P 비는 4.8 미만, 저층의 N:P 비는 3.8 미만이었다. 이는 N:P 비가 10 이하일 때에 M. polykrikoides가 주로 출현하였다는 이전 연구 결과와 일치한다(Tomas and Smayda[2008]). 2001년, 2015년, 2013년의 DIN 농도는 표층에서 각각 0.5, 0.1, 0.03 μM, 저층에서 각각 0.7, 0.1, 0.2 μM로, 이는 M. polykrikoides가 질소 고갈 환경에서 다른 종보다 더 잘 적응하고 생존에 유리하다는 사실을 의미한다(Kwon et al.[2014]).
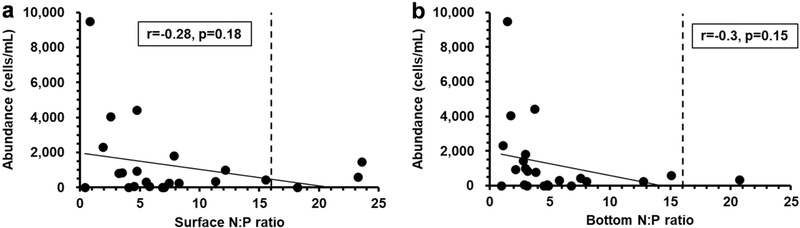
Correlations between M. polykrikoides maximum cell abundance and the N:P ratio. (a) surface, (b) bottom.
N:P:Si 비율을 분석한 결과, 1,000cells/mL 이상의 밀도로 발생한 M. polykrikoides 적조 중 개체수가 가장 높게 나타났던 2015년, 2013년, 2012년에는 표층과 저층 모두 N이 고갈되고 Si가 풍부한 환경에서 고밀도로 적조가 발생하였다(Fig. 7). 표층의 경우 N:P 비가 7.9 미만, N:Si 비가 0.04 미만인 환경에서, 저층의 경우에는 N:P 비가 3.8미만, N:Si 비가 0.02 미만인 환경조건에서 M. polykrikoides의 개체수가 높아졌다. 또한, 표층에 비해 저층이 더 제한된 환경 조건에서 고밀도 적조가 일어났다. 이는 표층보다 저층에서의 영양염 조건이 M. polykrikodies 개체수에 더 큰 영향을 끼침을 의미한다 (Baek et al.[2020]; Kwon et al.[2019]).
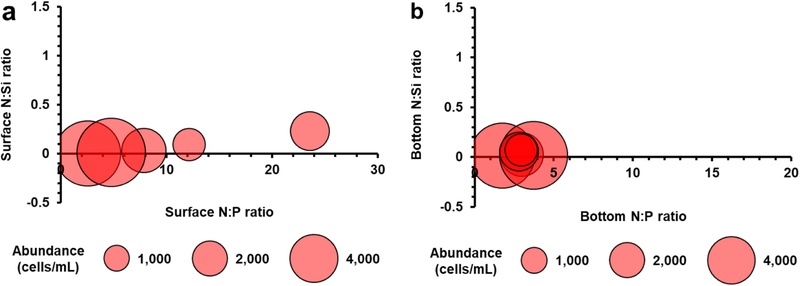
N:P:Si ratios under conditions where M. polykrikoides abundance exceeded 1,000 cells/mL. (a) surface, (b) bottom. Circle size represents cell abundance.
일반적으로 SiO2가 풍부한 환경에서는 규조류(diatoms)와 같은 다른 식물플랑크톤이 우점하여 M. polykrikoides의 성장을 제한할 수 있다(Lim et al.[2014]; Takano and Hino[1996]). 그러나 본 연구에서와 같이 SiO2 농도가 높음에도 불구하고 M. polykrikoides가 우점한 것은, 해당 시기에 규조류가 활발히 성장하지 않았음을 시사한다. 즉, 규조류가 충분히 존재한다면 SiO2를 빠르게 소모하여 저농도로 유지되었을 것이므로, SiO2가 높은 농도로 존재한다는 것은 규조류에 의해 SiO2가 소비되지 않았음을 의미하며, 이는 곧 규조류의 낮은 밀도를 반영한다. 따라서 SiO2가 풍부한 조건에서 M. polykrikodies는 경쟁자가 적은 환경에서 우위를 점하며, 고밀도 적조를 형성할 수 있다. 또한 질소 고갈이 동반될 경우, 규조류의 성장이 제한되면서 M. polykrikoides가 경쟁에서 우위를 차지한다. 이는 M. polykrikoides가 질소와 같은 필수 영양분이 부족한 환경에서도 혼합영양을 통해 성장을 유지할 수 있음을 시사한다(Hofmann et al.[2021]). 또한 대부분의 식물성 플랑크톤은 질산염이나 암모늄과 같은 무기 질소에 의존하지만 M. polykrikoides는 무기 질소 뿐만 아니라 다양한 유기 질소원도 효율적으로 이용하여 영양분이 부족한 환경에서도 유리한 생존 전략을 가진다(Al-Has et al.[2022]; Lee[2008]). 이러한 생리적 유연성을 통해 M. polykrikoides는 질산염이 고갈된 환경에서도 상대적으로 높은 생존율과 증식 잠재력을 유지할 수 있는 것으로 해석된다.
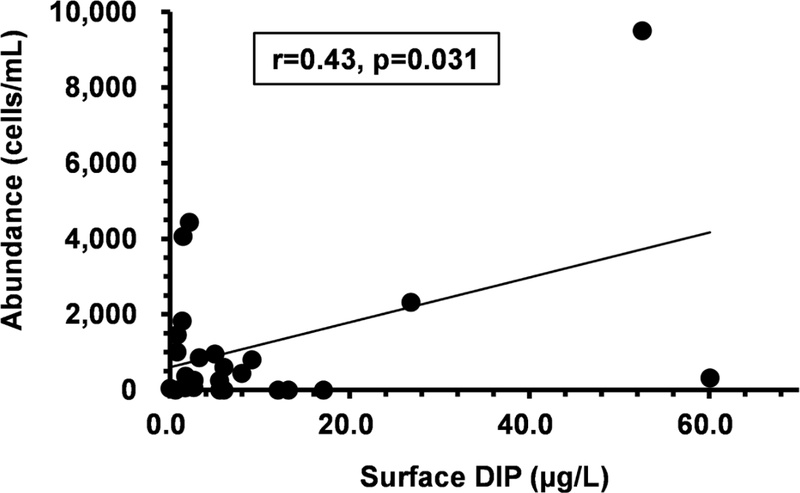
M. polykrikoides 적조의 개체수와 환경요인 간 상관관계를 분석한 결과, DIP를 제외한 다른 환경요인에서는 유의미한 관계를 확인하지 못하였다(unpublished data). 표층 DIP 농도는 개체수와 유의미한 양의 상관관계를 보였으며(r=0.43, p=0.031), DIP 농도가 높을수록 개체수도 증가하였다(Fig. 8). 반면에 표층 DIP 농도를 제외한 수온, 염분, DO, COD, NH4, NO2, NO3, DIN, TN, TP, SiO2, SS, Chl-a, 투명도 등 다른 환경요인들은 표층과 저층 모두 개체수와 유의미한 상관관계를 보이지 않았다(p>0.05). 이러한 결과는 M. polykrikoides의 성장에 있어 인이 중요한 제한 요인일 수 있음을 시사한다(Tomas and Smayda[2008]). 특히, 질소가 고갈된 환경에서는 상대적으로 풍부한 인이 M. polykrikoides의 생장을 촉진하는 핵심적인 요인이 될 수 있다(Rhee[1978]; Yuan et al. [2024]).
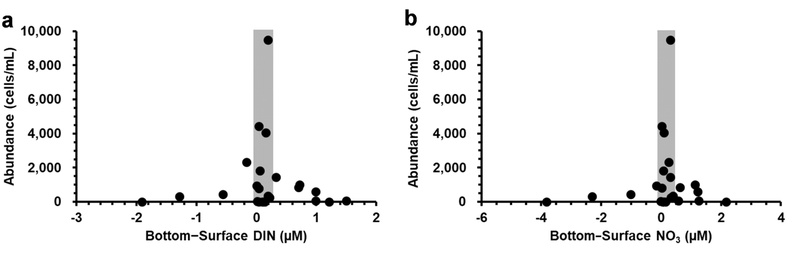
저층과 표층 간 영양염 농도 차를 분석한 결과, NH4, NO2, NO3, DIN, TN, DIP, TP의 농도 차가 0에 가까울수록 적조가 많이 발생하는 경향을 보였다. 특히 DIN과 NO3에서 이러한 경향이 두드러졌으며, 개체수가 가장 높았던 2001년, 2015년, 2013년, 2000년의 DIN 농도 차는 각각 24.5, 4.6, 19.5, -20.7μg/L, NO3 농도 차는 18.7, 0.8, 6.1, 15.8μg/L였다(Fig. 9). 기존의 연구들은 수층 성층화가 강할 때 M. polykrikoides가 저층의 영양염을 흡수하고 표층의 빛을 이용해 번성하는 수직 이동 능력을 활용하여 번성한다고 보고되었다(Clayton et al.[2024]; Lim et al.[2002]; Park et al.[2001]). 그러나 본 연구의 분석 결과는 DIN, NO3를 포함한 영양염의 표층과 저층 간 농도 차가 작을수록 M. polykrikoides의 개체수가 증가하는 경향이 나타나 기존 연구와는 다소 상반되는 결과를 보였다. 이는 표층과 저층에서 모두 영양염이 고갈된 환경에서 상대적으로 다양한 영양염 흡수 능력과 혼합영양 능력을 가지고 있는 M. polykrikoides가 이를 활용하여 필요한 영양분을 보충하며 영양염 고갈 환경에서 적응하였음을 시사한다(Hofmann et al.[2021]; Lim et al.[2022]; Park et al.[2001]). 본연구결과, 8월여수해역표층의 DIP 농도는 연도에 따라 유의하게 감소하는 반면, 표층과 저층 간의 DIP 농도 차이는 점차 확대되어 저층에서 상대적으로 높은 농도를 보였다. 이러한 경향이 지속되어 저층의 DIP 농도가 더욱 증가한다면, M. polykrikoides에 의한 유해성 적조 발생은 한층 심화될 것으로 예상된다.
3.5 여수 해역에서 M. polykrikoides 적조 발생 전망
본 연구 결과, 여수 해역의 표층 DIP 농도는 장기적으로 감소하는 추세를 보인 반면, 저층과 표층 간의 농도 차이는 점차 확대되어 저층에서 상대적으로 높은 DIP 농도가 유지되는 경향이 나타났다. 또한 M. polykrikoides는 질산염이 고갈되고 인산염이 풍부한 환경에서 높은 개체수를 보였으며, 표층과 저층 모두에서 낮은 N:P 비와 낮은 N:Si 비에서 대규모 적조가 형성되었다. 이러한 결과를 종합하면, 현재 나타나는 경향처럼 향후 저층의 DIP 농도가 더욱 높아질 경우, M. polykrikoides는 고밀도의 적조를 반복적으로 형성할 가능성이 크다. 따라서 여수 해역에서 M. polykrikoides에 의한 유해성 적조 발생은 단기적 변동성을 넘어 장기적으로 더욱 빈번하고 심화될 것으로 예측된다. 이를 검증하기 위해서는 향후 현장 조사를 통한 영양염 농도와 M. polykrikoides 적조 발생 및 밀도에 대한 지속적인 모니터링과 분석이 필요하다.
4. 결 론
본 연구는 M. polykrikoides 적조가 발생한 해역은 질산염이 고갈되고 규산염이 상대적으로 풍부한 환경이었으며, 질산염의 저층-표층 농도 차이가 작을 때 더욱 번성한다는 사실을 규명하였다. 또한 저층과 표층의 DIP 농도 차가 커질수록 M. polykrikoides에 의한 대규모 적조가 발생한다는 점을 밝혔다. 다만, 본 연구는 개체수와 영양염 농도를 동시에 측정한 자료가 아닌 장기 관측 데이터를 기반으로 하였으므로, 향후 현장에서의 동시 측정 연구를 통해 이러한 결과를 검증할 필요가 있다. 본 논문은 복합적인 영양염 비율 및 수직적 농도 차이 분석을 통해 적조 발생 메커니즘에 대한 새로운 통찰을 제공함으로써, 향후 적조 예측 모델의 정확도를 높이고 효과적인 관리 방안을 수립하는데 기여할 것으로 기대된다.
Acknowledgments
본 연구는 과학기술정보통신부의 재원으로 한국연구재단(NRF) 및 한국기초과학지원연구원 국가연구시설장비센터의 지원을 받아 수행되었음(RS-2025-16070437; RS-2024-00399598).
References
-
Al-Has, A., Mohammad-Noor, N., Muhamad Shaleh, S.R., Adam, A., Azrinor, W.A. and Weliyadi, E., 2022, Growth of harmful dinoflagellate Margalefidinium polykrikoides in different nutrient concentrations. Philipp. J. Sci., 151(3).
[https://doi.org/10.56899/151.03.13]

-
Anderson, D.M., Cembella, A.D. and Hallegraeff, G.M., 2012, Progress in understanding harmful algal blooms: paradigm shifts and new technologies for research, monitoring, and management. Ann. Rev. Mar. Sci., 4, 143-176.
[https://doi.org/10.1146/annurev-marine-120308-081121]

-
Anderson, D.M., Glibert, P.M. and Burkholder, J.M., 2002, Harmful algal blooms and eutrophication: nutrient sources, composition, and consequences. Estuaries, 25(4), 704-726.
[https://doi.org/10.1007/BF02804901]

-
Anderson, S.I., Barton, A.D., Clayton, S., Dutkiewicz, S. and Rynearson, T.A., 2021, Marine phytoplankton functional types exhibit diverse responses to thermal change. Nat. Commun, 12(1), 6413.
[https://doi.org/10.1038/s41467-021-26651-8]

-
Baek, S.H., Kim, Y., Lee, M., Ahn, C.Y., Cho, K.H. and Park, B.S., 2020, Potential cause of decrease in bloom events of the harmful dinoflagellate Cochlodinium polykrikoides in southern Korean coastal waters in 2016. Toxins, 12(6), 390.
[https://doi.org/10.3390/toxins12060390]

-
Baumert, H.Z. and Petzoldt, T., 2008, The role of temperature, cellular quota and nutrient concentrations for photosynthesis, growth and light–dark acclimation in phytoplankton. Limnologica, 38(3-4), 313-326.
[https://doi.org/10.1016/j.limno.2008.06.002]

-
Berdalet, E., Fleming, L.E., Gowen, R., Davidson, K., Hess, P., Backer, L.C., Moore, S.K., Hoagland, P. and Enevoldsen, H., 2016, Marine harmful algal blooms, human health and wellbeing: challenges and opportunities in the 21st century. J. Mar. Biol. Assoc. U. K., 96(1), 61-91.
[https://doi.org/10.1017/S0025315415001733]

-
Carney-Almeida, J., Sonnet, V., Mouw, C.B., Rines, J., Ciochetto, A.B. and Puggioni, G., 2024, Detecting Margalefidinium polykrikoides through high-frequency imagery: Example of a bloom formation, environmental conditions, and phytoplankton community composition changes. Harmful Algae, 136, 102619.
[https://doi.org/10.1016/j.hal.2024.102619]

-
Chang, W.K., Ryu, J., Yi, Y., Lee, W.C., Lee, C.W., Kang, D., Lee, C.H., Hong, S., Nam, J. and Khim, J.S., 2012, Improved water quality in response to pollution control measures at Masan Bay. Korea. Mar. Pollut. Bull, 64(2), 427-435.
[https://doi.org/10.1016/j.marpolbul.2011.11.011]

-
Clayton, S., Chrabot, J.B., Echevarria, M., Gibala-Smith, L., Mogatas, K., Bernhardt, P. and Mulholland, M.R., 2024, Diel vertical migration rates of the dinoflagellate species Margalefidinium polykrikoides in a lower Chesapeake Bay tributary. Front. microbiol., 15, 1378552.
[https://doi.org/10.3389/fmicb.2024.1378552]

-
de Silva, D. and Gobler, C.J., 2023, Effects of the harmful alga Margalefidinium (aka Cochlodinium) polykrikoides on clearance rates of the hard clam, Mercenaria mercenaria. Front. Mar. Sci., 10, 1252540.
[https://doi.org/10.3389/fmars.2023.1252540]

-
Dorantes‐Aranda, J.J., García‐de la Parra, L.M., Alonso‐Rodríguez, R., Morquecho, L. and Voltolina, D., 2010, Toxic effect of the harmful dinoflagellate Cochlodinium polykrikoides on the spotted rose snapper Lutjanus guttatus, Environ. Toxicol., 25(4), 319-326.
[https://doi.org/10.1002/tox.20507]

-
Falkowski, P.G., Barber, R.T. and Smetacek, V., 1998, Biogeochemical controls and feedbacks on ocean primary production. science, 281(5374), 200-206.
[https://doi.org/10.1126/science.281.5374.200]

-
Field, C.B., Behrenfeld, M.J., Randerson, J.T. and Falkowski, P., 1998, Primary production of the biosphere: integrating terrestrial and oceanic components. science, 281(5374), 237-240.
[https://doi.org/10.1126/science.281.5374.237]

-
Griffith, A.W., Doherty, O.M. and Gobler, C.J., 2019, Ocean warming along temperate western boundaries of the Northern Hemisphere promotes an expansion of Cochlodinium polykrikoides blooms. Proc. R. Soc. B, 286(1904), 20190340.
[https://doi.org/10.1098/rspb.2019.0340]

- Gyoon, K.H., Chang-Su, J.U.N.G., Wol, L.I.M., Sook-Yang, K.I.M., Sung-Hwa, Y.O.U.N. and Yong-Chul, C.H.O., 2001, The spatio-temporal progress of Cochlodinium polykrikoides blooms in the coastal waters of Korea. Korean J Fish Aquat Sci, 34(6), 691-696.
-
Heisler, J., Glibert, P.M., Burkholder, J.M., Anderson, D.M., Cochlan, W., Dennison, W.C., Dortch, Q., Gobler, C.J., Heil, C.A., Humphries, E., Lewitus, A., Magnien, R., Marshall, H.G., Sellner, K., Stockwell, D.A., Stoecker, D.K. and Suddleson, M., 2008, Eutrophication and harmful algal blooms: a scientific consensus. Harmful algae, 8(1), 3-13.
[https://doi.org/10.1016/j.hal.2008.08.006]

-
Hoagland, P. and Scatasta, S., 2006, The economic effects of harmful algal blooms. In Ecology of harmful algae (pp. 391-402). Springer, Berlin, Heidelberg.
[https://doi.org/10.1007/978-3-540-32210-8_30]

-
Hofmann, E.E., Klinck, J.M., Filippino, K.C., Egerton, T., Davis, L.B., Echevarría, M., Pérez-Vega, E. and Mulholland, M.R., 2021, Understanding controls on Margalefidinium polykrikoides blooms in the lower Chesapeake Bay. Harmful Algae, 107, 102064.
[https://doi.org/10.1016/j.hal.2021.102064]

-
Kim, D., Oda, T., Muramatsu, T., Kim, D., Matsuyama, Y. and Honjo, T., 2002, Possible factors responsible for the toxicity of Cochlodinium polykrikoides, a red tide phytoplankton. Comp. Biochem. Physiol. C, Toxicol. & Pharmacol, 132(4), 415-423.
[https://doi.org/10.1016/S1532-0456(02)00093-5]

-
Kim, D.I., Matsuyama, Y., Nagasoe, S., Yamaguchi, M., Yoon, Y.H., Oshima, Y., Imada, N. and Honjo, T., 2004, Effects of temperature, salinity and irradiance on the growth of the harmful red tide dinoflagellate Cochlodinium polykrikoides Margalef (Dinophyceae). J. Plankton Res, 26(1), 61-66.
[https://doi.org/10.1093/plankt/fbh001]

- Kim, Y.S., Jeong, C.S., Seong, G.T., Han, I.S. and Lee, Y.S., 2010, Diurnal vertical migration of Cochlodinium polykrikoides during the red tide in Korean coastal sea waters. J. Environ. Biol, 31(5), 687.
-
Kwon, H.K., Kim, G., Han, Y., Seo, J., Lim, W.A., Park, J.W., Park, T.G. and Han, I.S., 2019, Tracing the sources of nutrients fueling dinoflagellate red tides occurring along the coast of Korea using radium isotopes. Sci. Rep, 9(1), 15319.
[https://doi.org/10.1038/s41598-019-51623-w]

-
Kwon, H.K., Kim, H.J., Yang, H.S. and Oh, S.J., 2014, The Importance of Dissolved Organic Nutrients on the Interspecific Competition between the Harmful Dinoflagellate Cochlodinium polykrikoides and the Diatom Skeletonema sp. 1226-2978(pISSN), 19(4), 232-242.
[https://doi.org/10.7850/jkso.2014.19.4.232]

-
Lee, C.K., Park, T.G., Park, Y.T. and Lim, W.A., 2013, Monitoring and trends in harmful algal blooms and red tides in Korean coastal waters, with emphasis on Cochlodinium polykrikoides. Harmful Algae, 30, S3-S14.
[https://doi.org/10.1016/j.hal.2013.10.002]

-
Lee, D.K., 2008, Cochlodinium polykrikoides blooms and ecophysical conditions in the South Sea of Korea. Harmful Algae, 7(3), 318-323.
[https://doi.org/10.1016/j.hal.2007.12.014]

-
Lee, M.S., Park, K.A. and Kim, G., 2023, Incidence of harmful algal blooms in pristine subtropical ocean: a satellite remote sensing approach (Jeju Island). Front. Mar. Sci, 10, 1149657.
[https://doi.org/10.3389/fmars.2023.1149657]

-
Lee, Y.S., 2006, Factors affecting outbreaks of high-density Cochlodinium polykrikoides red tides in the coastal seawaters around Yeosu and Tongyeong, Korea. Mar. Pollut. Bull, 52(10), 1249-1259.
[https://doi.org/10.1016/j.marpolbul.2006.02.024]

- Lee, Y.S., 2008, Utilization of various nitrogen, phosphorus, and selenium compounds by Cochlodinium polykrikoides. J. Environ. Biol, 29(5), 799-804.
-
Lenzen, M., Li, M. and Murray, S.A., 2021, Impacts of harmful algal blooms on marine aquaculture in a low-carbon future. Harmful Algae, 110, 102143.
[https://doi.org/10.1016/j.hal.2021.102143]

-
Lim, A.S., Jeong, H.J., Jang, T.Y., Jang, S.H. and Franks, P.J., 2014, Inhibition of growth rate and swimming speed of the harmful dinoflagellate Cochlodinium polykrikoides by diatoms: implications for red tide formation. Harmful Algae, 37, 53-61.
[https://doi.org/10.1016/j.hal.2014.05.003]

-
Lim, W., Go, W.J., Kim, K.Y. and Park, J.W., 2020, Variation in harmful algal blooms in Korean coastal waters since 1970. J. Korean Soc. Mar. Environ. Saf, 26(5), 523-530.
[https://doi.org/10.7837/kosomes.2020.26.5.523]

-
Lim, Y.K., Kim, J.H., Ro, H. and Baek, S.H., 2022, Thermotaxic diel vertical migration of the harmful dinoflagellate Cochlodinium (Margalefidinium) polykrikoides: Combined field and laboratory studies. Harmful Algae, 118, 102315.
[https://doi.org/10.1016/j.hal.2022.102315]

-
López-Cortés, D.J., Núñez Vázquez, E.J., Dorantes-Aranda, J.J., Band-Schmidt, C.J., Hernández-Sandoval, F.E., Bustillos-Guzmán, J.J., Leyva-Valencia, I. and Fernández-Herrera, L.J., 2019, The state of knowledge of harmful algal blooms of Margalefidinium polykrikoides (aka Cochlodinium polykrikoides) in Latin America. Front. Mar. Sci, 6, 463.
[https://doi.org/10.3389/fmars.2019.00463]

-
Park, J., Kwon, Y.S., Baek, S.H., Lim, W.A., Park, J., Jang, J. and Park, Y., 2019, Identifying Environmental Effects on an Annual Variation in Margalefidinium polykrikoides in the South Korean Sea Using Statistical Analysis. J. Coast. Res, 90(SI), 11-18.
[https://doi.org/10.2112/SI90-002.1]

-
Park, J.G., Jeong, M.K., Lee, J.A., Cho, K.J. and Kwon, O.S., 2001, Diurnal vertical migration of a harmful dinoflagellate, Cochlodinium polykrikoides (Dinophyceae), during a red tide in coastal waters of Namhae Island, Korea. PHYCOL, 40(3), 292-297.
[https://doi.org/10.2216/i0031-8884-40-3-292.1]

-
Park, M.O., Lee, Y.W., Park, J.K., Kim, S.G., Kim, S.S. and Lee, S.M., 2018, Changes in water quality in Masan Bay after the introduction of the total pollution load management system. J. Korean Soc. Mar. Environ. Energy, 21(2), 139-148.
[https://doi.org/10.7846/JKOSMEE.2018.21.2.139]

- Park, T.G., Kim, J.J. and Song, S.Y., 2019, Distributions of East Asia and Philippines ribotypes of Cochlodinium polykrikoides (Dinophyceae) in the South Sea, Korea. 1226-2978(pISSN), 24(3), 422-428.
-
Park, T.G., Lim, W.A., Park, Y.T., Lee, C.K. and Jeong, H.J., 2013, Economic impact, management and mitigation of red tides in Korea. Harmful algae, 30, S131-S143.
[https://doi.org/10.1016/j.hal.2013.10.012]

-
Pérez-Vega, E., Mulholland, M.R., Crider, K.E., Powell, K.E., Chappell, P.D. and Bochdansky, A., 2025, The effect of temperature and salinity on Margalefidinium polykrikoides group III VA, USA strain growth. Harmful Algae, 102837.
[https://doi.org/10.1016/j.hal.2025.102837]

-
Rhee, G.Y., 1978, Effects of N: P atomic ratios and nitrate limitation on algal growth, cell composition, and nitrate uptake 1. Limnol. Oceanogr, 23(1), 10-25.
[https://doi.org/10.4319/lo.1978.23.1.0010]

-
Rolton, A., Rhodes, L., Hutson, K.S., Biessy, L., Bui, T., MacKenzie, L., Symond, J.E. and Smith, K.F., 2022, Effects of harmful algal blooms on fish and shellfish species: A case study of New Zealand in a changing environment. Toxins, 14(5), 341.
[https://doi.org/10.3390/toxins14050341]

-
Shin, J., Jo, Y.H., Ryu, J.H., Khim, B.K. and Kim, S.M., 2021, High spatial-resolution red tide detection in the southern coast of Korea using u-net from planetscope imagery. Sensors, 21(13), 4447.
[https://doi.org/10.3390/s21134447]

-
Sun, Y., Youn, S.H., Kim, Y., Kang, J.J., Lee, D., Kim, K., Jang, H.K., Jo, N., Yun, M.S., Song, S.K. and Lee, S.H., 2022, Interannual variation in phytoplankton community driven by environmental factors in the northern East China Sea. Front. mar. sci, 9, 769497.
[https://doi.org/10.3389/fmars.2022.769497]

-
Takano, K. and Hino, S., 1996, The effect of silicon concentration on replacement of dominant diatom [Bacillariophyceae] species in a silicon-rich lake. Jpn. J. Limnol, 57(2).
[https://doi.org/10.3739/rikusui.57.153]

-
Tomas, C. R. and Smayda, T.J., 2008, Red tide blooms of Cochlodinium polykrikoides in a coastal cove. Harmful algae, 7(3), 308-317.
[https://doi.org/10.1016/j.hal.2007.12.005]

-
Yang, H.J., Kim, Y.H., Seo, H.J., Lee, M.J. and Jang, S.H., 2024, Insights into plankton communities in a Margalefidinium polykrikoides (Gymnodiniales, Dinophyceae) bloom and adjacent non-bloom waters. Algae, 39(4), 277-291.
[https://doi.org/10.4490/algae.2024.39.12.10]

-
Yuan, Z., Achterberg, E.P., Engel, A., Dai, M. and Browning, T.J., 2024, Switches between nitrogen limitation and nitrogen–phosphorus co‐limitation in the subtropical North Atlantic Ocean. Limnol. Oceanogr, 69(4), 1005-1013.
[https://doi.org/10.1002/lno.12541]